Спочатку електронами заповнюється перший енергетичний рівень, потім другий, і тільки після остаточного заповнення другого енергетичного рівня розпочинається заповнення третього рівня. 2). У межах одного енергетичного рівня першим заповнюється s-підрівень, другим – p-підрівень.17 серп. 2020 р.
Підрівні оболонок позначаються літерами s, p, d, f, g, h, i або цифрами від 0 до 6.
На другому рівні вже два підрівні: s-підрівень (одна орбіталь) і p-підрівень (три орбіталі).
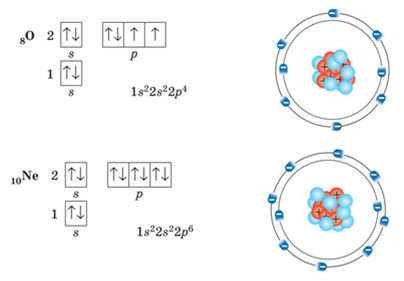
Електрони заповнюють енергетичні рівні в порядку послаблення притягання їх до ядра: спочатку s-, потім р-орбіталі, далі по одному, а якщо їх більше за число орбіталей, то по два, утворюючи електронні пари з протилежними спінами.
Число орбіталей на енергетичних рівнях різне, воно дорівнює п2, де п — номер рівня. На першому рівні (п = 1) одна s-орбіталь, на другому (п = 2) — чотири: одна s- і три р – орбіталі, на третьому (п = 3) – дев'ять: одна s-, три р- і п'ять d-орбіталей.
Ηλεκτρόνιο) — стабільна, негативно заряджена елементарна частинка, що входить до складу всіх атомів. Має електричний заряд (−e = −1,6021892(46)×10−19 Кл) і масу (9,109554(906)×10−31 кг).
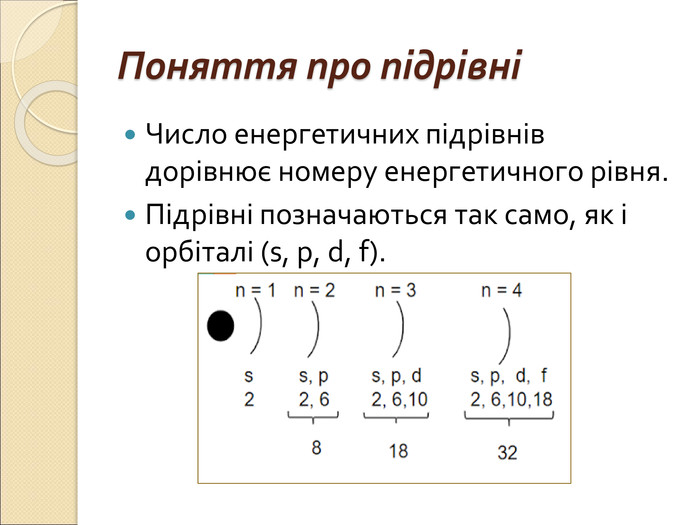
Енергетичні підрівні Кожний енергетичний рівень складається із підрівнів. Кількість підрівнів дорівнює номеру енергетичного рівня: перший рівень має один підрівень, другий — два, третій …